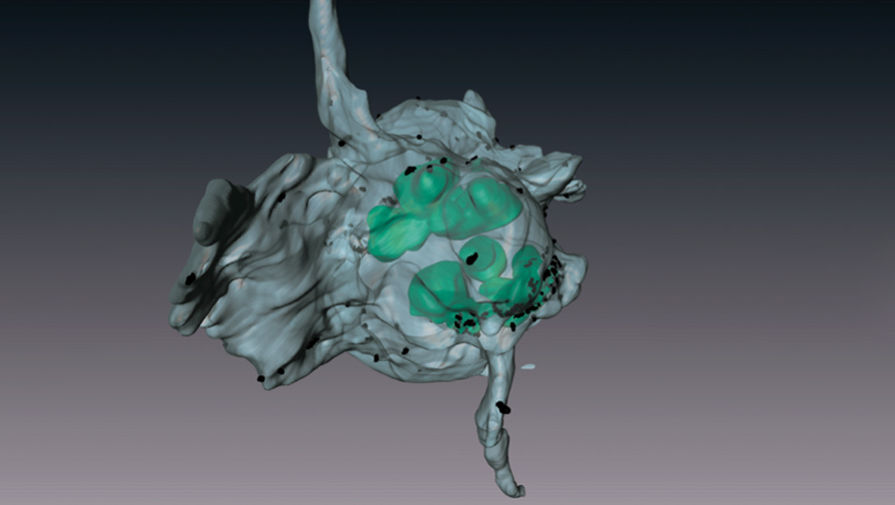
Зачем тромбоцитам «шапки»
«Шапки у тромбоцитов открыла наша команда в 2013 году, и с тех пор они стали признанным феноменом», — говорит Михаил Пантелеев.
Теперь ученые сделали еще один шаг к расшифровке проблемы свертывания крови: в новой статье, вышедшей в высокорейтинговом журнале Blood, они обнаружили, что в открытых ими ранее «шапках» находятся все ферменты, отвечающие за свертывание крови. Большинство авторов статьи — сотрудники МГУ им. М.В. Ломоносова. Работа шла в сотрудничестве с Федеральным научно-клиническим центром детской гематологии, онкологии и иммунологии (ФНКЦДГОИ) имени Дмитрия Рогачева, Центром теоретических проблем физико-химической фармакологии РАН и с Университетом Страсбурга. Исследования ученых поддержаны грантом Российского научного фонда (РНФ).
«Мы показали, что реакции свертывания крови протекают в «шапках» — специальных небольших структурах на поверхности тромбоцитов (клеток крови, которые отвечают за остановку кровотечения). Это нужно для того, чтобы ускорить эти реакции на два порядка (в 50–100 раз) и предотвратить вымывание ферментов свертывания из тромба», — рассказывает Михаил Пантелеев.
Вымывание ферментов свертывания опасно тем, что может вызвать тромбоз ниже по потоку крови, в результате чего становится возможным «затыкание» сосуда частью оторвавшегося тромба. Это явление, вызывающее ужас у всех, кто слышал о тромбозе, называется тромбоэмболия.
Для того чтобы предотвратить плачевные последствия, требуется полностью расшифровать механизм свертывания крови. Ученые постепенно объясняют этот процесс. Концентрация всех ферментов и разнообразных белков-посредников адгезии (закрепления клеток) в маленьком участке — «шапке» — на поверхности тромбоцита помимо ускорения реакций свертывания обеспечивает его прикрепление к растущему тромбу только в области «шапки». Это позволяет ферментам, которые могли бы вызвать сворачивание крови вне тромба, быть надежно спрятанными в теле тромба и недоступными для потока крови.
Сверхактивация или смерть
Процесс слипания тромбоцитов в результате повреждения кровеносных сосудов и образование прочных агрегатов для остановки кровотечений носит название гемостаз (от греч. haimatos — кровь, stasis — остановка). Он возможен в результате активации тромбоцитов. Активированные тромбоциты бывают разные: простые (агрегирующие) и сверхактивированные (прокоагулянтные). Простые агрегирующие тромбоциты формируют основное тело тромба. При активации они принимают амебовидную форму с множеством ножек для лучшего сцепления. Сверхактивированные тромбоциты большие и сферические, они увеличиваются в несколько раз по сравнению с неактивированным состоянием. Такой рост возможен за счет того, что у тромбоцита есть источник запасной мембраны — огромная сеть мембранных каналов внутри. Тромбоцит до активации пористый, как губка: он наполовину состоит из гранул и мембранных каналов, поэтому и может распухать.
Тромбоцит «узнает» о наличии повреждения с помощью разных активаторов, главные среди которых — коллаген, АДФ и тромбин. Коллаген — основной белок внеклеточного матрикса (трехмерной сетки молекул, отвечающей за соединение клеток в ткани организма). АДФ (аденозиндифосфат) – адениновый нуклеотид, содержащийся со всех клетках организма и участвующий в энергетике клеток. Тромбин является главным ферментом свертывания крови и вырабатывается в ходе гемостаза или тромбоза. В здоровом организме или при слабом повреждении тканей и органов активаторы не попадают в контакт с кровью, а при сильном их появление запускает процесс активации тромбоцитов, их слипания и образование тромба.
Активаторы стимулируют выброс ионов кальция Са2+ в цитоплазму тромбоцитов. Как было недавно показано Михаилом Пантелеевым с коллегами из МГУ им. М.В. Ломоносова в статье в Journal of Thrombosis and Haemostasis, митохондрии тромбоцита собирают кальций и, когда концентрация кальция в них достигает критической отметки, останавливают все жизненные (метаболические) процессы в тромбоците. Это значит, что тромбоцит умирает (из-за этого его называют «клетка-камикадзе»), тем самым переходя в сверхактивированное состояние. В нем прекращаются все процессы жизнедеятельности, он сильно увеличивается в размерах, раздувается — пустой, как пузырь. А ферменты, необходимые для ускорения реакций свертывания крови, оказываются сконцентрированными снаружи в маленькой «шапке».
Если есть сомнения, лучше свернуться
В целом система гемостаза имеет большой запас прочности. Она может быть «испорчена» генетическими заболеваниями, но это встречается редко. Самое знаменитое заболевание — гемофилия — встречается у одного человека из десятков тысяч, а остальные (например, тромбастения Гланцмана, когда тромбоциты не агрегируют) — у одного из миллиона или реже.
«В 50% случаев причина смерти заключается в том, что эта функция нашего организма (сворачивание крови) не рассчитана на современный образ жизни, и это приводит к смертности и инвалидности. Она не рассчитана на малоподвижный образ жизни, избыток жирной еды и хороший уровень медицины. Организм готов к тому, что человек много двигается в условиях недостатка еды и отсутствия медицины. Все, как у наших предков», — иронизирует Михаил Пантелеев.
В ряде случаев (в частности, при беременности, травмах, ожогах) процесс свертывания крови запускается «на всякий случай», что может приводить к закупориванию сосудов и тяжелым последствиям. Получается, что система гемостаза в организме срабатывает, когда современная медицина позволяет обойтись и без нее. При травмах теперь можно спасти человека, остановив кровотечение, но система активируется, и это может привести к смерти — парадоксально — от сворачивания крови при кровотечении.
Дисбаланс в системе гемостаза (и его следствие — образование тромбов) возникает за счет мутаций, онкологических заболеваний, инфекций, образования атеросклеротических бляшек и застойных зон крови, а также травм и ожогов. Отмечается, что атеросклероз (образование холестериновых бляшек на стенках артерий) является ведущей причиной смертности от тромбоза, ведь наш организм, подчеркивает автор исследования, не рассчитан на избыток жирной пищи, вся биохимия жирового обмена нацелена на запасание и перенесение голодных периодов.
«На протяжении всей истории человечества (кроме последнего века, может быть) опасность умереть до 20 лет от кровотечения или заражения крови была намного выше, чем от атеросклероза после 40 лет. Поэтому все наши защитные системы, включая гемостаз, исходно «выкручены на максимум». В результате сейчас большинство людей умирает от инфарктов и инсультов», — замечает Михаил Пантелеев.
Другой знаменитый тип тромбозов — венозные, во многом обязанные своим появлением зонам застоя в крови. Венозные тромбозы часто возникают как результат малоподвижного образа жизни, что проявляется в нарушении кровообращения.
«В ходе естественного отбора человек формировался в условиях, когда приходилось бегать, сражаться и работать физически. Природа не могла предвидеть офисной работы и многочасовых перелетов в самолете», — напоминает ученый.
В беседе Михаил Пантелеев подчеркнул, что эта работа (даже публикация статьи, о которой идет речь) была бы невозможной без поддержки проекта грантом РНФ, и объяснил почему.
«Про Российский научный фонд я могу говорить только с восторгом с момента его появления (даже до того, как я сам получил грант). Грант РНФ дал моей лаборатории в целом огромный толчок вперед. Иметь достойное финансирование на полноценные фундаментальные исследования — это совершенно другой уровень работы. В частности, статья в Blood стала возможной только благодаря РНФ. Достаточно сказать, что уже после принятия в печать одна только ее публикация (оплата page charges и цветных иллюстраций) стоила нам около 350 тыс. руб.. Причем статья в Blood — это ведь только часть большого проекта в рамках гранта РНФ, а у нас уже по этому гранту вышло более десяти интересных статей, и с каждой своя история поиска. С 2004–2005 годов в поддержке науки было много положительных сдвигов, которые заметны даже с моего уровня рядового ученого, но создание РНФ было качественным скачком», — рассказывает Михаил Пантелеев.
Текст подготовлен в сотрудничестве с проектом «Индикатор» (Indicator.Ru).